ルミネッセンス(発光)とは?
ATP測定の原理
ルミネッセンスとは何でしょうか。主な種類にはどのようなものがあるのでしょうか。また、どのように測定され、なぜライフサイエンス分野で重要視されているのでしょうか。本記事では、ルミネッセンスの定義、主な種類、発光の仕組みなどについて解説します。
ルミネッセンスとは何か ― 定義
ルミネッセンスとは、高温に起因しない光の放出現象を指します。そのため、この現象は「冷光(cold light)」とも呼ばれます。
私たちの身の回りには、さまざまな発光現象があります。これらは自然に発生するものと人工的に作り出されるものに分けられます。自然界におけるルミネッセンスの例としては、ホタルや植物プランクトンによる発光(生物発光)が挙げられます。一方、人工的なルミネッセンスの例としては、発光ダイオード(LED)やコンピューターモニター(エレクトロルミネッセンス)があります。

ルミネッセンスの種類
ライフサイエンス分野では、さまざまな種類のルミネッセンスが利用されています。ルミネッセンスは主に2つの観点から分類することができます。
① 高エネルギー状態の物質がどのように生成されるか(励起方法)
② 発光の持続時間
A. 高エネルギー物質の生成方法による分類
多くのルミネッセンスは、高エネルギー状態にある物質がエネルギーを光として放出する現象です。この高エネルギー状態がどのように生じるか、すなわちどのように「余分なエネルギー」を獲得するかという点は、ルミネッセンスを分類するうえで有用な基準となります。
1. 化学発光(Chemiluminescence)
化学発光とは、化学反応の結果として生じる発光現象を指します。反応エンタルピーが必要なエネルギーを供給し、励起状態の生成物または中間体が生じます。この中間体が基底状態へ戻る際に、光子(フォトン)を放出します。
生物発光(Bioluminescence)
このような反応がホタルのような生物体内で起こる場合、それは生物発光と呼ばれます。この生化学反応には、ルシフェリンと呼ばれる発光分子と、ルシフェラーゼと呼ばれる酵素が関与します。
ルシフェラーゼはフォトプロテインの一種であり、さまざまな昆虫、海洋生物、原核生物に存在します。これらの酵素はルシフェリンの酸化反応を触媒し、その結果として光子が放出されます。生物種によって酵素や基質、必要な補因子が異なるため、発光波長も異なります。その結果、発光スペクトルは約400 nmから620 nmの範囲に及びます。
ライフサイエンス分野で最も広く利用されているルシフェラーゼの一つはホタル由来ルシフェラーゼであり、約550~570 nmの黄緑色光を放出します。もう一つの代表例は、ウミシイタケ(Renilla reniformis)由来のレニラ・ルシフェラーゼであり、480~500 nmの青色光を放出します。
2. 光ルミネッセンス(Photoluminescence)
光ルミネッセンスとは、通常は紫外線や可視光によって物質が励起され(高エネルギー状態に移行し)、その結果として生じる発光現象を指します。この過程は「光励起」と呼ばれ、光子の吸収によって電子がより高いエネルギー準位へ移動することにより生じます。
励起後にはさまざまな緩和過程が起こり、一般的にはより低エネルギーの光子が再放出されます。光ルミネッセンスの主な種類は蛍光およびリン光です。蛍光特性を持つ分子はフルオロフォア(蛍光色素)と呼ばれます。ライフサイエンス分野では、蛍光アッセイにおいてこの形式のルミネッセンスが最も広く利用されています。
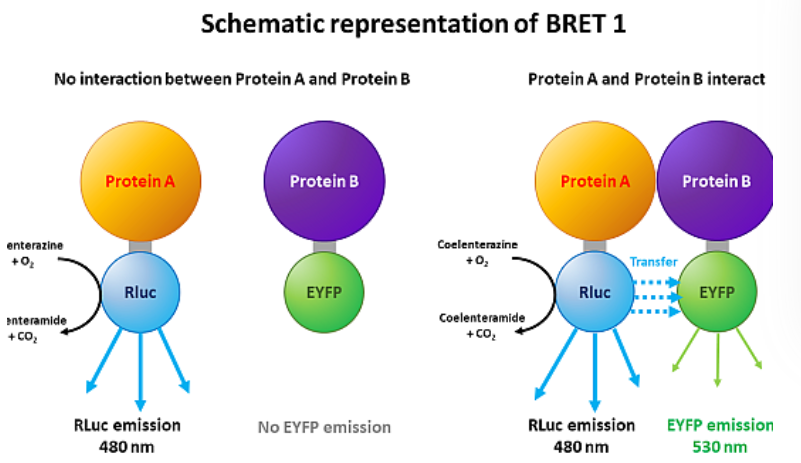
BRETおよびFRET
BRETおよびFRETは、エネルギー移動の特殊な形態を利用する手法であり、光ルミネッセンスの一種とみなすこともできます。いずれの方法も、ドナー分子とアクセプター分子という2つの分子(または分子群)を用います。
BRETではドナーはルシフェラーゼであり、FRETではドナーは蛍光色素です。アクセプターはいずれの場合も蛍光色素であり、ドナーの発光波長で励起される性質を持ちます。
アクセプターの励起は蛍光に類似していますが、BRETおよびFRETでは余剰エネルギーは放射を伴わない過程(非放射過程:virtual photon)によって移動します。これは、分子間の双極子‐双極子相互作用によって媒介される共鳴エネルギー移動と呼ばれます。
ここで用いられる「仮想光子(virtual photon)」という用語は、光子が実際の物理的特性(波長など)を持つ前に再吸収されることを示しています。
3. エレクトロルミネッセンス(Electroluminescence)
エレクトロルミネッセンスとは、物質に電流を流すことによって生じる発光現象を指します。ライフサイエンス分野では、主に一部のイムノアッセイや臨床応用における免疫化学で利用されています。
電気化学発光免疫測定法(ECLIA)は、非常に高感度な測定法です。この方法では、安定な前駆体(すなわちECL活性標識)から電極表面において電気化学的中間体が生成されます。その分子がより低いエネルギー準位へ戻る際に光を放出します。
4. ラジオルミネッセンス(Radioluminescence)
ラジオルミネッセンスは、特定の物質がα線、β線、γ線などの電離放射線を受けたときに発生する発光現象です。過去(1960年代頃)には、この現象は暗闇で光る時計の文字盤の製造に利用されていました。
この原理は、医薬および臨床分野のさまざまな用途において、高速液体クロマトグラフィー(radio HPLC)による放射性トレーサーの分離および検出にも応用されています。radio HPLCでは、電子がシンチレーター分子に衝突してそれを高エネルギー状態へ励起します。シンチレーターは直ちに元のエネルギー準位へ戻り、その際に光子を放出します。これらの光子は光電子増倍管(PMT)によって検出されます。
ライフサイエンス分野では、「ルミネッセンス」という用語は、蛍光よりもむしろ化学発光(およびそれに含まれる生物発光)を指して用いられることが一般的です。しかし、前述のとおり蛍光もルミネッセンスの一種です。
本分野における一般的な慣習に従い、本記事の以降の部分では、特に断りのない限り、「ルミネッセンス」という用語を化学発光および生物発光の意味で用いることにします。
B. 発光持続時間によるルミネッセンスの分類
1. フラッシュ発光(Flash luminescence)
短時間で発生し、通常は強いシグナルを示すアッセイは「フラッシュアッセイ」と呼ばれます。これらのアッセイのシグナル半減期は、一般的に数分程度、あるいはそれよりも短い場合があります。 フラッシュアッセイにおける課題は、試薬を添加するとシグナルがほぼ即座にピークに達し、その後急速に減衰する 点にあります。単一チューブ型ルミノメーターを使用する場合は、スターター試薬を添加した直後に各サンプルを個別に測定できるため、この点は問題になりません。しかし、マイクロプレート型ルミノメーターで測定する場合はど うでしょうか。96ウェルプレート内のすべてのウェルで同時に反応を開始し、 その後順番に測定した場合、最初のウェルのみがピーク強度で測定されることになります。一方、後から測定されるウェルでは、発光強度がすでに大幅に低下している可能性があります。そのため、マイクロプレートリーダーでフラ ッシュアッセイを測定する際には、いわゆるインジェクターの 使用が必要になります。これにより、各ウェルごとにスターター試薬を添加し、直ちにシグナルを測定することが可能になります。フラッシュタイプのアッセイの代表例としては、Dual- Luciferase Reporter™ アッセイや SPARCL アッセイが挙げられます。
2. グロー発光(Glow luminescence)
これに対して、グロータイプのアッセイは、数時間にわたって持続する発光シグナルを示します。シグナル強度自体はフラッシュタイプより低いものの、発光が長時間安定しているため試薬インジェクターを必要とせず、ワークフローが大幅に簡素化されます。そのため、このタイプのルミネッセンスアッセイが選択されることも少なくありません。
ただし、すべてのウェルが同時に発光しているため、隣接するウェルからの光が測定に影響を与える可能性があります。この現象は「クロストーク(crosstalk)」と呼ばれます(後述)。
ルミネッセンスの発光メカニズム
多くのルミネッセンスの発光機構は比較的単純です。光ルミネッセンスの場合は光子、エレクトロルミネッセンスの場合は電子といった粒子が電子に衝突し、それをより高いエネルギー状態へ励起します。その後、電子が基底状態へ戻る際に、余剰エネルギーが光として放出されます。
しかし、化学発光および生物発光の場合は、より複雑です。一般に、化学発光反応では、不安定で高エネルギー状態の中間体(多くの場合、ジオキセタノンまたはジオキセタン分子由来)が生成されます。この中間体が安定で低エネルギーの生成物へと変換される際、両者のエネルギー差が光として放出されます。ただし、この過程における化学結合の再配列や電子移動は非常に複雑であることが少なくありません。実際、数十年前から知られているいくつかの化学発光反応についても、その詳細な機構はごく最近になってようやく解明されました。
1. ルミノール発光のメカニズム
ルミノールの発光は、アルカリ条件下で分子状酸素の存在下において溶液中で観察されます。この反応では分子状窒素と励起状態の3-アミノフタレート二陰イオン(3AP²⁻)が生成されます。ルミノールの化学発光は、この励起一重項状態から基底状態への放射失活によって生じます。詳細な反応機構については、Giussani ら(2019)を参照してください。
2. ホタルルシフェラーゼ発光のメカニズム
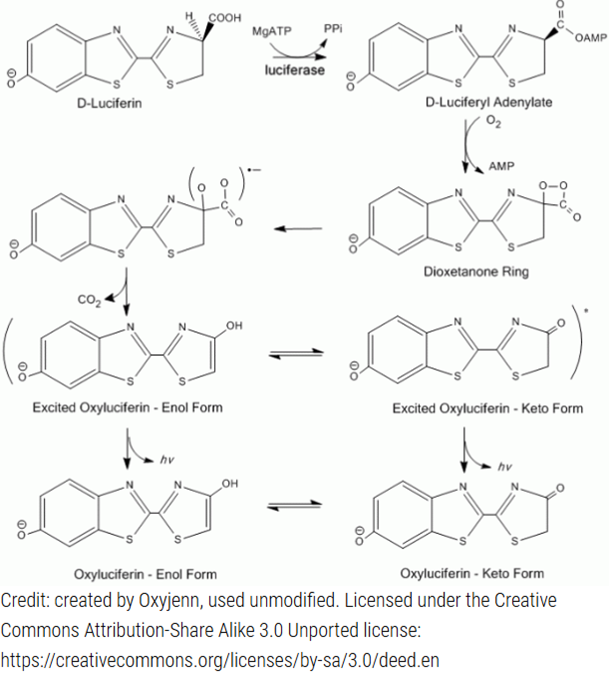
ホタルルシフェラーゼによる生物発光反応では、まず D-ルシフェリンと ATP-Mg²⁺ から D-ルシフェリル-AMP が生成されます。次に、この中間体はプロトンを失って反応性の高いカルバニオンを形成し、それが分子状酸素に対して求核攻撃を行い、ヒドロペルオキシドを生成します。その後、ヒドロペルオキシドがカルボニル基の求電子性炭素へ内部求核攻撃を行い、AMP が脱離基として放出されるとともに、エネルギーに富んだ環状ジオキセタノン構造が形成されます。このジオキセタノン環の酸化的脱炭酸反応により、発光分子であるオキシルシフェリンが生成されます。ジオキセタノン環は自発的に分解し(その詳細機構は完全には解明されていません)、一重項励起状態のオキシルシフェリンが生じます。この励起状態から基底状態へ戻る際に、可視光の光子が放出されます。
ルミネッセンスの利点
ルミネッセンス(すなわち化学発光および生物発光)に基づくアッセイは、吸光度測定など他の技術に基づくアッセイと比較して重要な利点を有しています。ただし、その利点は対象とするルミネッセンスの種類によって異なります。
ルミネッセンスアッセイは、非常に高い感度と広いダイナミックレンジを備えています。感度およびダイナミックレンジは、測定時のバックグラウンドが低く安定していることに大きく依存します。化学発光および生物発光アッセイでは、通常、目的分子以外に発光性物質が試料中に存在しないため、バックグラウンドは非常に低くなります。また、蛍光アッセイとは異なり、励起光を必要としないため、励起光に起因するバックグラウンドの増加もありません。
さらに重要な点として、ルミネッセンスアッセイで最も頻繁に使用される試薬は非危険性であることが挙げられます。放射性物質を用いるアッセイも優れた感度を有していますが、変異原性のリスクがあるため、その点でルミネッセンス法は安全性の面で優れています。
ルミネッセンスの限界
前述のとおり、最も高感度なルミネッセンスアッセイはフラッシュタイプであり、そのシグナル半減期は非常に短く(数分程度、あるいはそれ以下)、基質を分注するために自動試薬インジェクターを備えた装置が必要になります。
また、同一試料を複数回測定すること(例えば異なる測定条件や装置を比較する場合)は容易ではありません。再測定のたびに新たな基質を添加する必要があり、その結果、試料が希釈され、マイクロプレートやチューブの最大容量を超える可能性があります。
一方、グロータイプのアッセイでは、シグナルの半減期が長く(通常は数時間)、自動インジェクターを備えた装置は必須ではありません。しかし、新たな問題としてクロストークが生じる可能性があります。クロストークとは、あるウェルのシグナルを測定している際に、隣接ウェルからの光が漏れて検出器に到達する現象です。
もし隣接ウェルのシグナルが測定対象ウェルよりもはるかに強い場合、この不要な光によって測定値が過大評価される可能性があり、誤った結果につながるおそれがあります。クロストークの詳細およびその最小化方法については、別途参照してください。
また、生物発光および化学発光では異なる発光波長を持つ系が存在しますが、利用可能な波長の選択肢は比較的限られており、発光スペクトルの帯域幅も比較的広いという特徴があります。そのため、同一試料中で複数のシグナルを同時に検出するマルチプレックスアッセイの設計は困難です。マルチプレックス化には、一般に蛍光法のほうが適しています。
ルミネッセンスの測定
ルミネッセンスは、通常ルミノメーターを用いて測定されます。ルミノメーターの主要構成要素は、光電子増倍管(PMT)および暗室です。ルミネッセンス測定に使用される装置については、別途詳しく解説されています。
ルミネッセンスの強度は、通常 RLU(Relative Light Units:相対発光単位)で表されます。
推奨製品
装置:プレートリーダー、チューブルミノメーター、in vivoイメージングシステム (Berthold Technologies製)
この実験系には下記の装置が最適です!



