Vibrio fischeri を用いた固体試料および有色試料の毒性測定のための動的(キネティック)発光細菌試験
固体試料および有色水試料の毒性測定は、従来、時間を要し、実施が困難で、かつ信頼性に課題があった。水試料の濃い暗色や、固体試料における細菌の沈降、濁度および色度が、測定上の問題を引き起こしていたためである。フラッシュ法(Flash Method)は、これらの明らかな問題点を克服することを目的として設計された手法であり、さらに多くの利点を有する。本法は極めて迅速であり、試料によっては30秒以内に結果が得られる。フラッシュ法は、生物発光性細菌 Vibrio fischeri を利用した BioTox™ 試験に基づいている。色度および濁度の影響は試料ごとに自動的に補正されるため、複雑な推定計算を必要としない。測定は、試薬の分注と同時に測定が可能な装置を用い、動的(キネティック)モードで実施される。測定は Vibrio fischeri 試薬を試料に分注することにより開始され、これにより発光強度は急激に増加する。発光強度の最大値(ピーク値)は通常1~2秒以内に到達する。このピーク高さは、試料の色度および濁度に反比例する。毒性算出のための第2の測定値(エンドポイント値)は、15分または30分後に測定される。試料の毒性は、エンドポイント値とピーク値の比として算出される。得られた結果は、無毒性参照試料(2% NaCl 溶液)から求めた補正係数を用いて補正される。
試薬(Reagents)
・Vibrio fischeri 試薬
・試薬希釈液
・試料希釈液(20% NaCl)
・pH調整用 0.1 M NaOH および HCl
測定装置(Luminometer)
・ディスペンサー1基を備えた Sirius (チューブルミノメーター)
ソフトウェア(Software)
・Sirius PC ソフトウェア
インキュベーター(Incubator)
・15℃
その他の材料(Other Materials)
・ルミノメーター用キュベット(75 mm × 12 mm φ)
・一般的な実験室用機器:
天秤、ミキサー、pHメーター、ワイドチップ付きピペット、チューブ
Sirius PC ソフトウェアのプロトコル設定
試薬注入後の動的(キネティック)測定を行うため、ディスペンサー1基を備えた Sirius ルミノメーターを使用した。
ピーク値測定用シングル・キネティックプロトコル
・ディレイ時間:1.0 秒
・総測定時間:5.0 秒
・サンプリング時間:1.0 秒
・データポイント数:25
・インターバル時間:0.2 秒
・測定開始条件:ドアクローズ時にタイマー開始
・リプリケート数:1
エンドポイント測定用クイック測定プロトコル
・ディレイ時間:1.0 秒
・測定時間:0.2 秒
試験手順
試薬の調整
冷凍庫から Vibrio fischeri 試薬を取り出した直後に、冷却した(3℃ ± 3℃)試薬希釈液を Vibrio fischeri 試薬バイアルに全量加える。調整した試薬は、少なくとも30分間、+4℃で平衡化させる必要がある。測定開始のおよそ1時間前に、細菌懸濁液を測定温度(15℃)に移す。調整後の試薬は当日中に使用しなければならず、保存することはできない。1バイアルの内容量は、約35回の測定に相当する。
試薬の調製
1)試料作成
・固体試料
別々のチューブにおいて、試料2.0gを2% NaCl 溶液(試料希釈液の1/10希釈)8.0mLに加え、5分間撹拌する。
・水試料
試料9mLに20% NaCl 溶液1mLを加えて塩分濃度を調整し、穏やかに混和する。
2)pHを測定し、pHが6~8.5の範囲外にある場合は、7.0 ± 0.2に調整する。
3)各試料を2% NaCl 溶液で希釈し、適切な段階希釈系列(例:1:2、1:4、1:8、1:16)を調製する。
4)2% NaCl 溶液を対照試料として使用する。
注記
試料の毒性レベルが全く不明な場合には、未希釈試料、1/10希釈、1/100希釈試料などを用いたスクリーニング/レンジファインディング試験を事前に実施することが推奨される。
生物発光測定
1)試料および各段階希釈試料(対照試料を含む)を十分に混合し、それぞれ300µLをルミノメーター用チューブに分注する。
測定前に、15℃で少なくとも10分間インキュベーションする。
2)ディスペンサーの分注量を300µLに設定し、Vibrio fischeri 試薬でディスペンサーのプライミングを行う。
3)最初の試料を装置にセットし、シングル・キネティックプロトコルを用いて測定を開始する(細菌試薬が試料に分注され、発光強度が5秒間キネティックモードで追跡される)。測定後、試料を15℃のインキュベーターに戻し、一定の時間間隔を保ちながら、すべての試料について同様の操作を繰り返す。最大発光強度(Smax)を取得する。
4)混合直後に、15分および/または30分後の発光強度を測定する。クイック測定プロトコルを使用し、15分後および/または30分後の発光強度(S15min および/または S30min)を取得する。
計算および結果の解釈
阻害率および EC50 値の算出は、ISO 規格に従って実施する。ただし、初期発光強度として、純粋な細菌懸濁液の初期発光値の代わりに Smax を用いる点が唯一の例外である。
試料の毒性は、S15min/Smax および S30min/Smax の比を算出することにより評価する。
S/Smax の比が 0.8 未満の場合、当該試料は通常、毒性を有すると判断される。これらの S/Smax 比は、試料濃度に対してプロットすることができる。このプロットから、EC20 および EC50 値(発光をそれぞれ20%および 50%阻害する濃度)を求めることが可能である。
注記
試料のピーク高さが対照試料の 10%未満である場合には、試料をさらに希釈しなければならない。
例
図1は、キネティック測定の原理を示している。図2は、発光の時間変化における有毒試料と無毒試料の違いを示している。曲線Aは、毒性および吸光の影響が認められない正常な挙動を示す。曲線Bは、吸光の影響を伴わないが強い毒性を有する試料を示している。曲線Cは、毒性と吸光の両方の影響を含む試料を示している。曲線Dでは、毒性作用を伴わない非常に強い吸光効果が確認される。
図1:キネティック毒性測定の基本的な模式プロトコル
(キー:1.測定開始、2.細菌注入、3.0~5秒間のピーク値記録、試料を混合後、30分後の信号を記録)
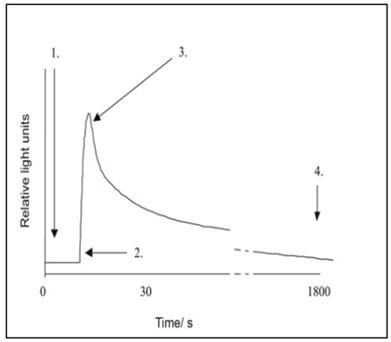
図2:
有毒試料および無毒試料における代表的なキネティック挙動
(キー:A:透明で無毒性の試料、B:透明で毒性を有する試料、C:濁度または着色を有し、毒性を示す試料、D:濁度または着色を有するが無毒性の試料)


推奨製品
装置:チューブルミノメーター (Berthold Technologies製)
この実験系には下記の装置が最適です!